A partir da experiência adquirida junto a clientes e parceiros, o Laboratório CENIC identificou que as maiores dificuldades em relação ao relatório técnico exigido como um dos documentos do registro da Anvisa são:
• Não apresentar ensaios para comprovação da segurança e eficácia;
• Não realizar ensaio no caso mais crítico (pior caso);
• Apresentar ensaios parciais sem avaliação crítica;
• Ausência de análise crítica.
A partir dessas dificuldades, o Laboratório CENIC através da ATRIO, sua nova unidade de negócio, passou a oferecer, dentre outros serviços, Rotas de Ensaios e Assessoria em Análise Crítica de resultados.
O acerto na escolha dos ensaios e uma análise crítica adequada minimizam as dificuldades na obtenção do grande objetivo final: o registro do produto.
Apresente sua necessidade regulatória. Teremos total atenção e dedicação para seu sucesso regulatório na ANVISA Este endereço de email está sendo protegido de spambots. Você precisa do JavaScript ativado para vê-lo. | 16 3371-5490
Rotas de Ensaios
As Rotas de Ensaios são caminhos organizados que auxiliam a economizar recurso financeiro e tempo no momento de definir os ensaios a serem realizados para comprovação da segurança e eficácia. Nelas serão encontradas para cada implante ortopédico, as normas de ensaios aplicadas de cada órgão normativo (ASTM, ISO, NBR), inclusive com indicação de normas equivalentes entre si.As rotas definem ensaios que se aplicam ao produto de maneira mais direta, sem correr o risco de não abranger todos os ensaios ou realizar ensaios similares de órgãos normativos diferentes.
O acerto na escolha dos ensaios e uma análise crítica adequada minimizam as dificuldades na obtenção do grande objetivo final: o registro do produto.
Para entender melhor como funcionam as rotas, veja abaixo uma Rota orientativa dos ensaios necessários para um sistema de coluna:
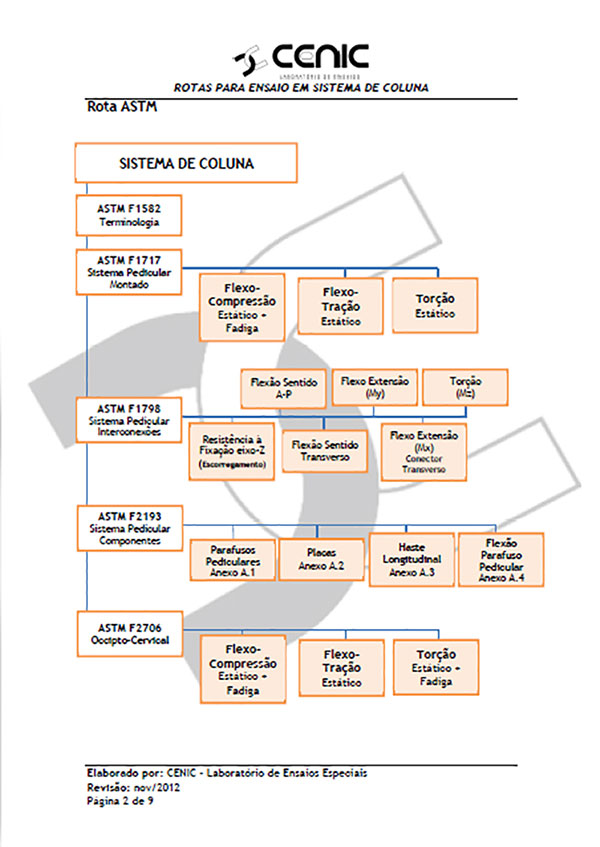
Análise Crítica
O que é e para que serve a análise crítica?As agências regulatórias, de um modo geral, exigem que seja comprovada a segurança e eficácia de um implante ortopédico. Dessa forma, fabricantes e importadores responsáveis pelo registro de um determinado produto, precisam não apenas apresentar resultados de ensaio, mas também interpretar e contextualizar os resultados obtidos para o seu produto, indicando por meio de uma análise crítica se o produto é seguro e eficaz.
Cada agência regulatória tem suas peculiaridades, mas todas esperam alguma discussão dos resultados de ensaio. Essa discussão pode ser baseada em comparações de resultados de trabalhos científicos, de literatura técnica de desenvolvimento, cálculos biomecânicos e outras fontes de consulta.
ESCLARECIMENTO SOBRE O RESPONSÁVEL DA ANÁLISE CRÍTICA:
O Regulamento técnico anexo à RDC nº 185 de 22/10/01 estabelece em sua Parte 3, item 5b, que as informações descritas nos Anexos III.A, III.B e III.C devem ser declaradas e assinadas pelo responsável técnico.
O Anexo III.C define as informações do relatório técnico. O item 1.6 do Anexo III.C, mais especificamente, trata da comprovação da segurança e eficácia, que deve ser conduzida com base na RDC nº 56/2001, que estabelece os requisitos essenciais de segurança e eficácia aplicáveis aos produtos para saúde.
Declarar e assinar afirmações se o produto é seguro e eficaz a partir de resultados de ensaios, é uma das ferramentas comumente utilizadas como comprovação de segurança e eficácia. Portanto, conforme definido pela RDC nº 185, é competência do responsável técnico e não do Laboratório de ensaios fazer tais afirmações.





